Анемия у кошек: причины, виды, лечение и профилактика
Анемия – это состояние, характеризующееся уменьшением количества эритроцитов и гемоглобина в крови. Гемоглобин связывает кислород и доставляет его к каждой клетке, поэтому недостаток гемоглобина…
Анемия – это состояние, характеризующееся уменьшением количества эритроцитов и гемоглобина в крови. Гемоглобин связывает кислород и доставляет его к каждой клетке, поэтому недостаток гемоглобина приводит к кислородному голоданию.
Богатая кислородом кровь имеет ярко-красный цвет, а кровь с недостатком кислорода – более темный. Это также влияет на внешний вид человека – кожа становится бледной, как бы "кровоточащей".
Кстати, греческий корень слова "анемия" и означает "бескровный".
Основные причины анемии
Специалисты выделяют три основные причины анемии:
- Массовая гибель эритроцитов или анемия с повышенной кровоточивостью;
- недостаточное производство эритроцитов костным мозгом или анемия с нарушением кроветворения;
- Большая кровопотеря.
Как правило, первая из названных причин имеет генетическое происхождение – врожденные заболевания, такие как серповидно-клеточная анемия. Более распространенной является анемия, вызванная чрезмерной кровопотерей или недостаточным производством эритроцитов. Все виды анемии имеют свои причины и методы лечения.
Дефицит железа
Железодефицитная анемия – самый известный и наиболее распространенный тип.
При дефиците железа костный мозг производит маленькие, бледные эритроциты, которые содержат мало гемоглобина.
Это приводит к дефициту кислорода в организме, что вызывает сильную слабость и недомогание, одышку, головокружение, головные боли и частые ощущения холода, из-за которых трудно оставаться в тепле.
Предупреждение. Железо играет важную роль в регуляции температуры тела, и его дефицит приводит к неспособности сохранять тепло.
Существует множество причин железодефицитной анемии, включая наиболее распространенные, такие как недостаточное поступление железа с пищей, плохое усвоение железа, беременность, скачок роста в период полового созревания и другие.
У женщин запасы железа также ниже, чем у мужчин: доказано, что почти 20% женщин детородного возраста и 50% беременных женщин страдают этим видом анемии.
Вегетарианцы и приверженцы жестких диет также подвержены высокому риску развития анемии, если их ежедневный рацион не обогащен "зелеными" источниками железа, которое содержится в шпинате, брокколи и др.
Кровотечение
При длительном или незамеченном кровотечении вместе с кровью может быть потеряно большое количество эритроцитов.
Часто такие скрытые кровотечения обусловлены заболеваниями желудочно-кишечного тракта: язвами, геморроем, гастритом, раком желудка.
Хронические кровотечения также могут возникать при приеме некоторых нестероидных противовоспалительных препаратов, например, аспирина. И, конечно, самая банальная причина, касающаяся женщин – менструация и роды.
Витамин B₁₂
Язвенная анемия – классическое проявление дефицита витамина B₁₂ в организме. Помимо железа, витамин B₁₂ необходим для образования красных кровяных телец. Ткани костного мозга и нервной системы особенно уязвимы к дефициту этого витамина.
Характерным симптомом витаминодефицитной анемии или авитаминоза является образование в костном мозге аномально больших клеток, которые не могут превратиться в эритроциты и погибают в костном мозге. Язвенная анемия чаще встречается у взрослых и связана с атрофией желудка. Самым богатым пищевым источником витамина B₁₂ является печень.
Впервые B₁₂ был выделен из нее в 1934 году, и это открытие было удостоено Нобелевской премии по медицине.
Предупреждение. Гангренозную анемию можно обнаружить с помощью обычного анализа крови.
Фолиевая кислота
Фолиевая кислота – еще один важный фактор для успешного производства красных кровяных телец. Она также защищает стенки кровеносных сосудов от повреждения, укрепляет сердечно-сосудистую систему и предотвращает развитие сердечных приступов. Такие продукты, как молоко, яйца, мясо, морепродукты и птица, являются источниками витамина B₁₂ и фолиевой кислоты.
Анемия, вызванная разрушением красных кровяных телец
Другой тип анемии вызван разрушением красных кровяных телец – эритроцитов. К ним относятся гемолитическая анемия, аутоиммунная анемия, серповидноклеточная анемия и талассемия. При гемолитической анемии, например, разрушение красных кровяных телец происходит быстрее, чем костный мозг успевает их вырабатывать. Это может быть обусловлено генетически, а в некоторых случаях вызвано инфекциями или некоторыми лекарствами. Даже стрессовые ситуации, такие как укусы насекомых или даже определенные продукты питания, могут спровоцировать развитие гемолитической анемии. При аутоиммунной гемолитической анемии иммунная система атакует собственные эритроциты, принимая их за чужеродные организмы. Этот вариант заболевания может быть спровоцирован различными факторами – раком, сильными ожогами, воздействием химических веществ.
Серповидноклеточная анемия также вызвана разрушением красных кровяных телец. Когда они в норме, они круглые и мягкие по форме, легко проходят по кровеносным сосудам и доставляют кислород ко всем тканям организма.
Серповидные клетки намного жестче и имеют неправильную форму, поэтому они могут застревать в мелких кровеносных сосудах и препятствовать нормальному току крови. Организм уничтожает эти "неправильные" клетки, но не успевает вырабатывать новые в необходимом количестве, что приводит к анемии.
Это заболевание обычно вызывается генетическим дефектом.
Апластическая анемия возникает из-за неспособности организма вырабатывать достаточное количество красных кровяных телец.
При этой анемии в костном мозге мало или совсем нет клетообразующей ткани. Она может быть вызвана рентгеновскими лучами и некоторыми лекарствами.
Апластическая анемия также передается по наследству. Это серьезное заболевание, требующее немедленного лечения антибиотиками.
Диета как средство лечения
Для лечения и профилактики анемии рекомендуется щадящий режим труда и отдыха, диета, богатая животным белком и витаминами, а также ограничение жиров. Рекомендуется включать в рацион достаточное количество продуктов, содержащих легко усваиваемое железо. К таким продуктам относятся:
- говядина;
- телятина;
- кровяная колбаса;
- печень;
- субпродукты;
- рыба;
- яичный желток.
Важно помнить, что мясные блюда следует сочетать с овощами и фруктами, богатыми витамином С, так как этот витамин помогает нашему организму усваивать железо.
Аскорбиновая кислота и витамины группы В содержатся в картофеле, капусте, баклажане, кабачках, дыне, тыкве, шиповнике, облепихе, ежевике, клюкве, боярышнике, крыжовнике, лимоне, апельсине, абрикосе, вишне, груше, кукурузе и др.
Например, съев на обед говяжьи отбивные, выпейте на десерт стакан апельсинового сока.
Внимание!!! Растительная пища также содержит железо, но оно не так легко усваивается.
Однако можно несколько пополнить запасы железа в организме, употребляя темно-зеленые овощи, картофель, тыкву, свинину, лук, чеснок, укроп, крыжовник и виноград.
Кроме того, в качестве вспомогательных средств и поддерживающей терапии при анемии рекомендуются богатые аскорбиновой кислотой ягоды черной смородины, рябины, шиповника и листья земляники лесной.
Из ягод и листьев этих растений готовят витаминный чай.
Не забывайте, что одной диеты недостаточно для здоровья вашей семьи. Не забывайте, что одной диеты часто бывает недостаточно и необходимо принимать специальные лекарства. Чтобы узнать, какие лекарства вам необходимы, пройдите медицинское обследование и обсудите лечение со своим врачом.
Анемия
ЧТО ТАКОЕ АНЕМИЯ?
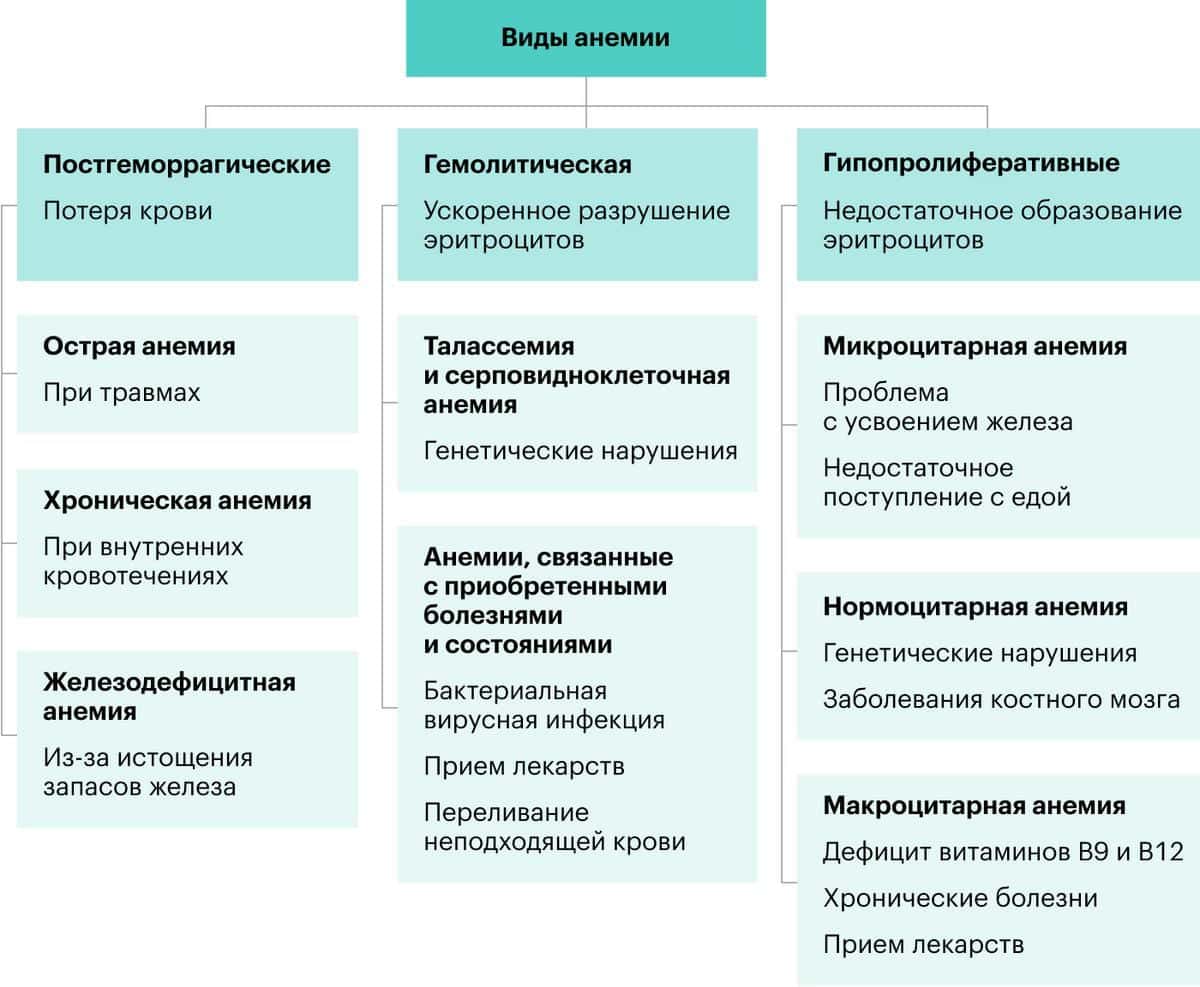
Анемия — это состояние, характеризующееся снижением концентрации гемоглобина (ниже 130 г/л у мужчин и 120 г/л у женщин) и гематокрита (ниже 39% у мужчин и 36% у женщин). Обычно также наблюдается уменьшение количества красных кровяных телец (эритроцитов).
Различные виды анемии встречаются у 10-20% населения, в основном у женщин.
Наиболее распространенными являются анемии, вызванные дефицитом железа (около 90% всех анемий), реже встречаются анемии, вызванные хроническими заболеваниями, и еще реже – анемии, вызванные дефицитом витамина В12 или фолиевой кислоты (мегалобластические), гемолитические и апластические анемии. Важно помнить, что анемия может иметь сложное происхождение. Возможно сочетание железодефицитной анемии и дефицита В12.
КЛАССИФИКАЦИЯ АНЕМИЙ
В клинической практике чаще всего используется следующая классификация анемий:
- Анемия вследствие острой кровопотери
- Анемия, вызванная нарушением выработки эритроцитов
- Апластическая
- Железодефицитная
- Мегалобластическая
- Сидеробластическая
- Хронические заболевания
- Анемия вследствие повышенного разрушения эритроцитов
В зависимости от тяжести падения уровня гемоглобина различают три степени анемии:
- Легкая – Уровень гемоглобина выше 90 г/л;
- Умеренная – Уровень гемоглобина от 90 до 70 г/л;
- Тяжелая – Гемоглобин ниже 70 г/л.
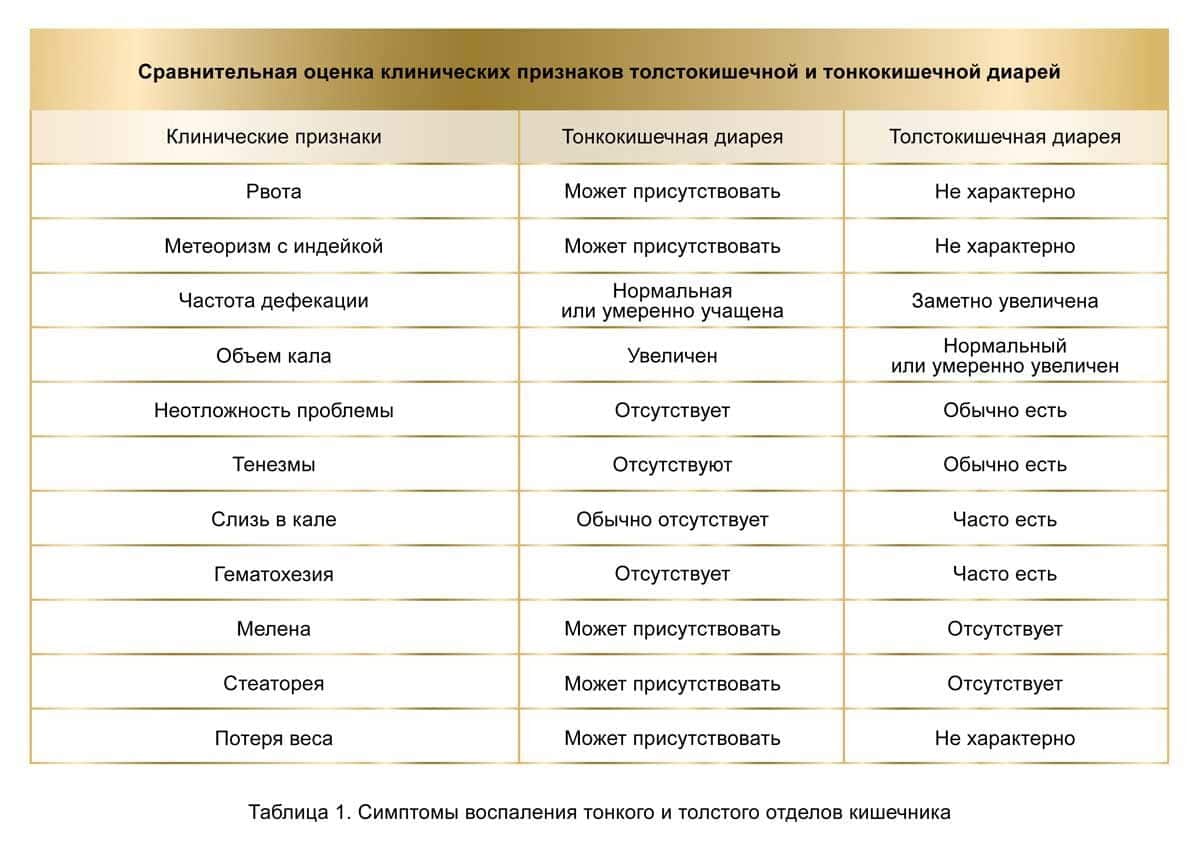
ОБЩИЕ СИМПТОМЫ АНЕМИИ
- Слабость, повышенная утомляемость, снижение работоспособности, раздражительность, вялость
- Головокружение, головная боль, шум в ушах, мелькание "мушек" перед глазами,
- учащенное сердцебиение при незначительной нагрузке или в покое
- Одышка при незначительной нагрузке или в состоянии покоя.
Часто первой жалобой пожилых пациентов с ишемической болезнью сердца является учащение приступов стенокардии даже после легкой нагрузки. Тяжесть анемии различна и зависит от типа и степени тяжести анемии, скорости возникновения и личности пациента.
ДИАГНОСТИКА АНЕМИИ
Анемия может быть диагностирована путем:
- медицинского обследования
- Общий клинический анализ крови с обязательным определением:
- Количество эритроцитов
- количество ретикулоцитов
- Гемоглобин
- Гематокрит
- Средний объем эритроцитов (MCV)
- Ширина распределения объема красных клеток (RDW)
- Средний гемоглобин в эритроцитах (MCH)
- Средняя концентрация гемоглобина в эритроцитах (MCHC)
- Количество лейкоцитов
- Количество тромбоцитов
- Для более детальной диагностики конкретных видов анемии используются дополнительные методы исследования.
- ЖЕЛЕЗОДЕФИЦИТНАЯ АНЕМИЯ
- ДИАГНОСТИКА
- Для диагностики железодефицитной анемии необходимы дополнительные анализы:
- Определение уровня сывороточного железа.Определение уровня сывороточного железа, ферритина и насыщенного трансферрина; определение общей железосвязывающей способности и ненасыщенного трансферрина.
- Аспирационная биопсия костного мозга не является обязательным тестом для диагностики железодефицитной анемии и проводится только при наличии особых показаний.
ОСНОВНЫЕ ПРИНЦИПЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ
- Устранение причины дефицита железа.
- Диета, богатая железом (мясо, печень и т.д.).
- Длительное лечение железом (4-6 месяцев).
- Парентеральное введение железа (при наличии показаний).
- Переливание красных кровяных телец в случаях тяжелой анемии.
- Профилактический прием препаратов железа в группах риска.
- B12-ДЕФИЦИТНАЯ АНЕМИЯ
- ДИАГНОСТИКА
- Для диагностики В12-дефицитной анемии необходимы дополнительные исследования:
- Определение уровня витамина B12 в крови.
- Аспирационная биопсия Аспирационная биопсия костного мозга (если невозможно определить уровень витамина В12 в крови или если нет ответа на лечение в течение 5-8 дней).

- ОСНОВНЫЕ ПРИНЦИПЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ
- Заместительная терапия.
- Сбалансированная диета.
- ФОЛАТДЕФИЦИТНАЯ АНЕМИЯ
- ДИАГНОСТИКА
- Для диагностики фолатдефицитной анемии необходимы дополнительные исследования:
- Определение уровня фолиевой кислоты в сыворотке крови и эритроцитах.
- Показания к проведению Аспирационная биопсия костного мозга такие же, как и при В12-дефицитной анемии.
ОСНОВНЫЕ ПРИНЦИПЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ
- Профилактическое назначение фолиевой кислоты Беременные пациенты; пациенты, принимающие противосудорожные и некоторые другие препараты.
- Назначение терапевтической дозы фолиевой кислоты при заместительной терапии
.
- АНЕМИЯ ПРИ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЯХ
- ДИАГНОСТИКА
- Для диагностики анемии при хронических заболеваниях необходимы дополнительные анализы:
- Определение уровня сывороточного железа, общей железосвязывающей способности и насыщения трансферрина, уровня сывороточного ферритина, уровня эритропоэтина в крови.
- Аспирационная биопсия костного мозга проводится при наличии показаний.
- Исследования для выявления основного заболевания, вызвавшего анемию.
- ОСНОВНЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ
- Лечение основного заболевания.
- Лечение рекомбинантным эритропоэтином
- Введение фолиевой кислоты в случае дефицита фолиевой кислоты.
- ПРИОБРЕТЕННАЯ ГЕМОЛИТИЧЕСКАЯ АНЕМИЯ
- ДИАГНОСТИКА
- Для диагностики приобретенной гемолитической анемии необходимы дополнительные исследования:
- Определение свободного и связанного билирубина в сыворотке крови и моче.
- Определение осмотической резистентности эритроцитов.
- Проведение прямого теста Кумбса.
- ОСНОВНЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ
- Глюкокортикостероиды.
- Спленэктомия (удаление селезенки).
- Иммуносупрессивные препараты.
- Антилимфоцитарный глобулин.
- Плазмаферез.
Как правило, вышеперечисленные методы лечения приобретенной гемолитической анемии применяются последовательно. Плазмаферез является дополнительным и может сопровождать любое медикаментозное или хирургическое лечение.
При тяжелых формах заболевания, не поддающихся вышеуказанному лечению, может проводиться высокодозная иммуносупрессивная терапия с последующим введением колониестимулирующих факторов и/или гемопоэтических стволовых клеток.
- АПЛАСТИЧЕСКАЯ АНЕМИЯ
- КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
- Клинические проявления апластической анемии, особенно в ее тяжелых и крайних формах, помимо общих симптомов, характерных для всех анемий, сходны с таковыми при остром лейкозе:
- кровотечение
- восприимчивость к инфекциям
- ДИАГНОСТИКА
- Для диагностики апластической анемии необходимы дополнительные исследования:
- Аспирационная биопсия костного мозга (цитологическое исследование)
- Трепанационная биопсия костного мозга (гистологическое исследование)
- Цитогенетическое исследование костного мозга и клеток периферической крови.
ОСНОВНЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ:
Лечение пациентов с тяжелой и крайне тяжелой апластической анемией начинается сразу после подтверждения диагноза.
Терапия должна проводиться в специализированной гематологической больнице, имеющей необходимый опыт и оборудование. Размещение должно быть в палатах не более чем на 2 человека, с туалетом и душем.
Вентиляция важна для того, чтобы обеспечить быстрое удаление из воздуха микробов, опасных для пациентов с апластической анемией.
Основными методами лечения апластической анемии являются:
- Аллогенная трансплантация костного мозга – при наличии родственного донора.
- Комбинированное иммуносупрессивное лечение (антилимфоцитарный глобулин – при наличии родственного донора). (антилимфоцитарный или антитимоцитарный глобулин, сандиммун).
- Заместительная терапия компонентами крови (эритроциты, тромбоциты),
- Профилактика и лечение инфекционных осложнений (антибактериальная, противогрибковая и противовирусная терапия).
Апластическая анемия
Апластическая анемия
МКБ-10
D6060.-D6161.
МКБ-10-КМ
D61.9, D61.2, D61.3, D61.8, D61.1 и D61.0
МКБ-9
284284
МКБ-9-КМ
284.9[1][2] и 284.
8[2]
OMIM
609135
DiseasesDB
866
MedlinePlus
000554
eMedicine
med/162
MeSH
D000741
Апластическая анемия – Анемия – это нарушение кровообращения, характеризующееся голоданием костного мозга с недостаточной продукцией эритроцитов, лейкоцитов и тромбоцитов (пангемоцитопения) или только эритроцитов (частичная гипопластическая анемия, синонимы: пангемоцитопения): апластическая анемия, арегенеративная анемия, геморрагический лейкоз, миелопарез, миелофитоз, панмиелофитоз, прогрессирующий гипоцитоз). Апластическая анемия характеризуется выраженной панцитопенией – анемией, лейкопенией, тромбоцитопенией и лимфопенией[3].
История болезни
Впервые заболевание было описано Паулем Эрлихом в 1888 году у 21-летней женщины. Термин "апластическая анемия" был введен Шофордом в 1904 году. Апластическая анемия является одним из самых тяжелых нарушений гемопоэза. Без лечения пациенты с тяжелыми формами апластической анемии умирают в течение нескольких месяцев.
При своевременном и адекватном лечении прогноз достаточно благоприятный. Долгое время апластическую (гипопластическую) анемию рассматривали как синдром, сочетающий патологические состояния костного мозга с выраженной гипоплазией кроветворения.
Современная медицина классифицирует апластические анемии как арегенераторные (гипо-, апластические) анемии[4].
Этиология
Апластическая анемия может быть вызвана:
- Химические вещества (мышьяк, ароматические углеводороды, особенно бензол, соли тяжелых металлов).
- Ионизирующее излучение (см. Мари Склодовская-Кюри).
- Лекарства (НПВС, цитостатики, мерсиколил, анальгетики, левомицетин).
- Инфекционные агенты (вирусы, м/о).
- Аутоиммунные процессы (СКВ, синдром Шёгрена).
Патогенез
Апластическая анемия может развиться после воздействия ряда миелотоксических агентов: ионизирующего излучения, химических веществ – бензола, солей золота, мышьяка; лекарственных препаратов – хлорамфеникола (левомицетина), фенилбутазона (бутадиона), хлорпромазина (аминазина), мепробамата, дилантина, антиметаболитов (6меркаптопурина, метотрексата), алкилирующих препаратов (циклофосфата, хлорбутина) и некоторых других. Миелотоксическое действие некоторых агентов (ионизирующее излучение, антиметаболиты) проявляется всегда при достаточно высокой дозе, других – индивидуально. Причина индивидуальной чувствительности, особенно к некоторым препаратам, не всегда ясна, но может быть связана с генетическими дефектами гемопоэтических клеток. Это относится, например, к хлорамфениколу и фенилбутазону, которые вызывают подавление (в зависимости от дозы) эритропоэза с частотой 1:24 000 и 1:40 000, соответственно, у людей, принимающих их.
Наследственный характер индивидуальной чувствительности эритропоэтических клеток к этим препаратам подтверждает развитие аплазии костного мозга у разных членов одной семьи и у однояйцевых близнецов. В других случаях лекарственное подавление кроветворения может быть связано с иммунологическими механизмами через появление антител против предшественников эритроцитов. Случаи апластической анемии были описаны после острого вирусного гепатита (вероятно, из-за способности вируса гепатита изменять кариотип клеток, что было прослежено в культуре лейкоцитов), инфекции вирусом Эпштейна-Барр, парвовирусной инфекции.
Существует также наследственная форма апластической анемии – анемия Фанкони.
Более чем у половины пациентов причинные факторы не могут быть идентифицированы – это известно как идиопатическая апластическая анемия. Механизмы, лежащие в основе идиопатической анемии, неясны.
Возможным аутоиммунным механизмом является воздействие аутоантител на клетки костного мозга с участием иммунных лимфоцитов.
Было показано, что лимфоциты (Т-супрессоры) пациентов подавляют образование колоний донорских эритроцитов костного мозга и могут нарушать дифференцировку и пролиферацию гематопоэтических предшественников.
Также было высказано предположение, что изменение (внутренний дефект) стволовой клетки может лежать в основе апластической анемии, о чем свидетельствует восстановление кроветворения у пациентов после аллогенной трансплантации костного мозга, содержащего нормальные стволовые клетки.
Существуют экспериментальные доказательства важности для развития апластического процесса и микроэкологических аномалий – первичного дефекта стволовых клеток костного мозга. Однако природа этих клеточных дефектов остается неясной, как и их первичная природа.
Возможно, что патогенетические механизмы различны при разных формах апластической анемии.
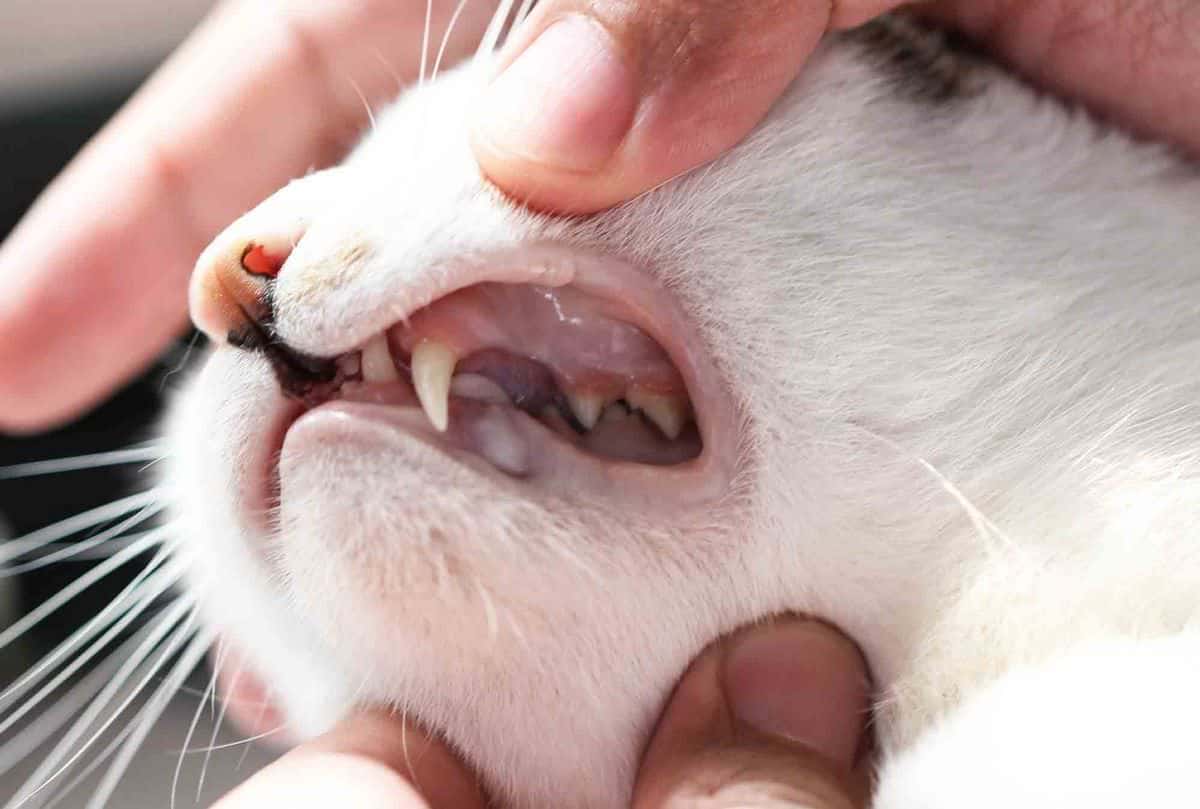
Клиническая картина
- Анемический синдром (головокружение, снижение трудоспособности, утомляемость, бледность кожи и слизистых оболочек, сердцебиение, непереносимость длительной физической нагрузки и т.д.).
- Геморрагический синдром (кровотечения, склонность к диапедезу, кровоизлияния).
- Инфекционные осложнения.
Диагностика
Картина периферической крови представляет собой трицитопению. Падение гемоглобина значительное и может достигать критического уровня 20 – 30 г/л. Цветовой показатель обычно один, но в некоторых случаях может наблюдаться гиперхромия и макроцитоз эритроцитов.

Количество ретикулоцитов сильно снижено. Характерна тяжелая лейкопения (агранулоцитоз). Абсолютное количество лимфоцитов не изменено или снижено. Количество тромбоцитов всегда снижено, в некоторых случаях их вообще не удается обнаружить.
В большинстве случаев наблюдается увеличение скорости оседания (до 40-60 мм/ч).
Клиническая картина заболевания является начальным признаком патологии кровообращения. Отправной точкой диагностического поиска является клинический анализ крови с определением количества ретикулоцитов и тромбоцитов. Обнаружение би- или трицитопении в периферической крови является основанием для проведения морфологического исследования костного мозга.
Диагноз АА ставится на основании типичной гистологической картины костного мозга, полученной при трепанационной биопсии подвздошного гребня. Коммерчески доступные (Sherwood medical) трепанационные биопсии используются для получения высококачественной (информативной) биопсии.
Гистологическое исследование костного мозга выявляет большое количество жировой ткани, которое может достигать 90%. Среди преобладающей жировой ткани преобладают стромальные и лимфоидные элементы. Гематогенные клетки представлены крайне скудно: эритроидные и гранулоцитарные предшественники присутствуют в небольшом количестве. Мегакариоциты отсутствуют.
Лечение
Лечение апластической анемии – очень сложная задача.
- Лечение глюкокортикоидами эффективно, если заболевание обусловлено аутоиммунными механизмами, антителами против клеток крови.
- Лечение анаболическими препаратами стимулирует кроветворение.
- Лечение андрогенами оказывает анаболическое действие и стимулирует эритропоэз.
- Лечение цитостатиками (иммуносупрессивными препаратами) – назначается только при безуспешности других методов лечения у пациентов с аутоиммунными заболеваниями, включая частичную аплазию эритроцитов.
- Спленэктомия
- Лечение антилимфоцитарным глобулином рекомендуется, если спленэктомия и другие методы лечения оказались безуспешными.
- Лечение циклоспорином. Циклоспорин А (сандиммун) оказывает иммуносупрессивное действие, избирательно ингибирует транскрипцию гена интерлейкина-2 в Т-лимфоцитах, подавляет выработку интерферона гамма и фактора некроза опухоли альфа.
- Трансплантация костного мозга.
Основным и единственным патогенетическим методом лечения апластической анемии, позволяющим надеяться на спасение жизни пациента, является трансплантация костного мозга от совместимого донора.
Если донора найти не удается, проводится паллиативное лечение. В качестве основного препарата используется иммуносупрессивный препарат циклоспорин А.
У пациентов с нетяжелой апластической анемией применение этого препарата в некоторых случаях может быть эффективным.
Кроме того, циклоспорин А полезен, поскольку глюкокортикоиды, андрогены и антилимфоцитарный глобулин могут улучшить гемопоэз у пациентов с нетяжелой апластической анемией, но при этом следует учитывать повышенный риск последующего клонального заболевания костного мозга. Циклоспорин А сводит этот риск к минимуму.
Следует также отметить, что у некоторых пациентов с нетяжелой апластической анемией, превысивших порог 6-месячной выживаемости, состояние может улучшиться спонтанно, даже если они не получают никакого иммуносупрессивного лечения. Эффект иммуносупрессивного лечения у пациентов с тяжелой и крайне тяжелой апластической анемией сомнителен.
- Лечение колониестимулирующими факторами или миелоидными факторами роста – это гликопротеины, которые стимулируют пролиферацию и дифференцировку различных типов гемопоэтических клеток-предшественников.
- Переливание эритроцитов; показания: тяжелая анемия, церебральная гипоксия, гемодинамические нарушения.
Все пациенты с апластической анемией нуждаются в заместительной трансфузионной терапии эритроцитами и/или тромбоцитами. Объем трансфузионной терапии определяется показателями периферической крови и клиническими проявлениями заболевания. Кроме того, для профилактики или лечения инфекционных осложнений проводится антимикробная и микостатическая терапия.
Прогноз
Ремиссия достигается примерно у половины всех пациентов. Прогноз у детей несколько лучше, чем у взрослых. Большое количество жира в костном мозге не означает, что процесс необратим.
Известны случаи, когда полная ремиссия и полное восстановление костномозгового кроветворения происходят даже у таких пациентов.
Прогноз лучше, когда количество ретикулоцитов повышено, когда в костном мозге наблюдается более полиморфная картина, когда есть небольшое увеличение селезенки и когда есть хотя бы небольшой, но выраженный эффект кортикостероидных гормонов.
В этих случаях спленэктомия чаще приводит к хорошему исходу вплоть до полного излечения. У некоторых пациентов апластический синдром является началом острого лейкоза. Иногда симптомы гемобластоза обнаруживаются только через несколько лет после начала заболевания.
Примечания
- ↑ Disease Ontology release 2019-05-13 – 2019.
- ↑ 1 2 Monarch Disease Ontology release 2018-06-29sonu – 2018-06-29 – 2018.
- ↑ Y. I. Laurier, F. E. Feinstein. ГИПОПЛАСТИЧЕСКАЯ АНЕМИЯ // Большая медицинская энциклопедия : в 30 томах / под ред. В. Petrovsky. – В 3 т. – Москва : Советская энциклопедия, 1977 г. – Т. 5. гипотиазид. – 568 с. – 150 000 экз.
- ↑ Чеснокова Н.П., Неважай Т.А., Моррисон В.В., Бисенкова М.Н.. ЛЕКЦИЯ 2. АНЕМИИ: КЛАССИФИКАЦИЯ, ОБЩАЯ ХАРАКТЕРИСТИКА ГЕМАТОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ. ПОСТГЕМОРРАГИЧЕСКАЯ АНЕМИЯ // Международный журнал прикладных и фундаментальных исследований : статья. – 2015. – № 6-1. – С. 152-155. – ISSN 1996-3955 ISSN 1996-3955.
| В статье отсутствуют ссылки на источники информации.Информация должна быть проверяемой, иначе она может быть оспорена и удалена.Вы можете редактировать эту статью, добавляя ссылки на авторитетные источники.Эта отметка установлена 26 октября 2017 г.. |